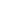对PD-L1的去泛素化和稳定作用可应用于肿瘤生物治疗
虽然炎症的先天反应对宿主免疫防御至关重要,但癌症细胞在慢性炎症环境中通常会产生T细胞抵抗,这被称为癌症的第七个特征,有助于血管生成、癌症细胞进展、侵袭和转移。临床研究表明,炎症性疾病患者患结直肠癌、食道癌、胰腺癌、肝癌和乳腺癌的风险显著增加。
先天免疫介导的炎症在癌症生物学中的作用仍存在争议。然而,在大多数情况下,炎性细胞因子如肿瘤坏死因子(TNF)或IL-6已被证明可增强肿瘤生存、增殖或血管生成。此外,通过某些细胞因子、代谢产物和膜受体的表达,巨噬细胞和髓系衍生抑制细胞可以抑制适应性抗肿瘤反应,抑制肿瘤微环境中的效应免疫反应是肿瘤逃逸的中心机制。在过去的十年中,免疫检查点的概念已经通过鉴定几种使效应免疫偏向耐受的分子途径而出现。其中,B7/CTLA-4和PD-L1/PD-1通路对CD4和CD8 T细胞的抑制引领了癌症治疗的新方法,即免疫检查点阻断。针对这两种途径的抗体已证明在黑色素瘤和癌症中具有良好的临床疗效。

Programmed death ligand 1(PD-L1,也称为B7-H1或CD274)是B7家族的一种跨膜蛋白,由多种癌症细胞和肿瘤浸润免疫细胞(包括树突状细胞和巨噬细胞)表达。PD-L1与T细胞表面的受体PD-1结合,抑制增殖、存活和效应细胞因子如IFN-γ或IL-2的分泌,这最终导致T细胞耗竭。除了对T细胞的这种直接影响外,有人提出,肿瘤细胞中的PD-L1信号传导可能通过维持最佳代谢谱来促进其增殖和存活。许多癌症通过表达PD-L1逃避免疫监测,PD-L1与其受体PD-1相互作用,导致T细胞增殖和活化减少,随后T淋巴细胞介导癌症细胞死亡。
肿瘤微环境中产生的促炎性细胞因子可消除抗肿瘤免疫并提高肿瘤细胞存活率。Lim等人观察到巨噬细胞来源的TNF通过增加PD-L1蛋白表达而不改变mRNA水平来增强免疫抑制和肿瘤生长。通过质谱实验,他们证明由NF-κB p65诱导的COP9信号体5(CSN5)是TNF-α介导的PD-L1稳定癌症细胞所必需的。CSN5鉴定为TNF诱导的PD-L1结合蛋白,CSN5的C-末端结构域与PD-L1结合后,去除了PD-L1上K48连接的泛素,从而提高PD-L1蛋白的稳定性。CSN5 mRNA的表达由TNF模拟诱导,并依赖于NF-κB亚基RelA/p65,后者通过结合其启动子直接调节CSN5的表达,因此可以说,CSN5抑制PD-L1的泛素化和降解。
转录因子NF-κB家族被广泛描述为炎症、肿瘤增殖和细胞生存途径的中枢调节因子。因此,人们投入了大量精力来识别NF-κB通路抑制剂以治疗癌症。然而,全身NF-κB阻断导致的不良副作用阻碍了其临床发展。目前的研究重申了一些有效的NF-κB抑制剂的治疗潜力,并表明这种抑制剂与检查点阻断疗法联合使用可能特别有效。此类方法的安全性至关重要,某些已知具有低毒性的天然分子,如姜黄素,通过其对NF-κB和CSN5的抑制降低了癌症细胞PD-L1的表达,并使癌症细胞对CTLA4的治疗更敏感,可能是有效的癌症治疗方法,且副作用有限。
关键词:
治疗,细胞,癌症,pd-l1,肿瘤,免疫,通过,nf-&kappa,表达,抑制
上一页:
下一页:
热线:400-963-0063
手机:13353108343
邮箱:2478535005@qq.com
地址:长春市北湖科技开发区盛北大街3333号北湖科技园B区E9栋